GIỚI THIỆU VỀ HỢP CHẤT HỮU CƠ - LÝ THUYẾT
GIỚI THIỆU VỀ HỢP CHẤT HỮU CƠ
I. HỢP CHẤT HỮU CƠ, HÓA HỌC HỮU CƠ
1. Khái niệm hợp chất hữu cơ
- Hợp chất của cacbon gọi là hợp chất hữu cơ (trừ CO, CO₂, muối cacbonat, muối cacbua…).
- Hợp chất hữu cơ có vai trò quan trọng trong đời sống:
+ Ở người, động vật, thực vật: hợp chất hữu cơ tham gia vào quá trình sống.
+ Carbohydrat, protein, lipid, vitamin là hợp chất hữu cơ thiết yếu trong dinh dưỡng.
2. Ví dụ một số hợp chất hữu cơ phổ biến
- Butan (C₄H₁₀): khí hóa lỏng, làm nhiên liệu.
- Rượu etylic (C₂H₅OH): có trong đồ uống có cồn.
- Axit axetic (CH₃COOH): thành phần chính của giấm.
- Ure [CO(NH₂)₂]: phân đạm.
- Đường saccarozơ (C₁₂H₂₂O₁₁): đường tinh luyện.
- Cacbon tetraclorua (CCl₄): dung môi hữu cơ.
Kết luận
- Hóa học hữu cơ nghiên cứu về thành phần, cấu tạo, tính chất và ứng dụng của hợp chất hữu cơ.
- Hợp chất hữu cơ chiếm đa số trong tự nhiên và có vai trò quan trọng trong đời sống.
2. Phân loại hợp chất hữu cơ
Dựa vào thành phần phân tử, các hợp chất hữu cơ được chia thành hai loại chính:
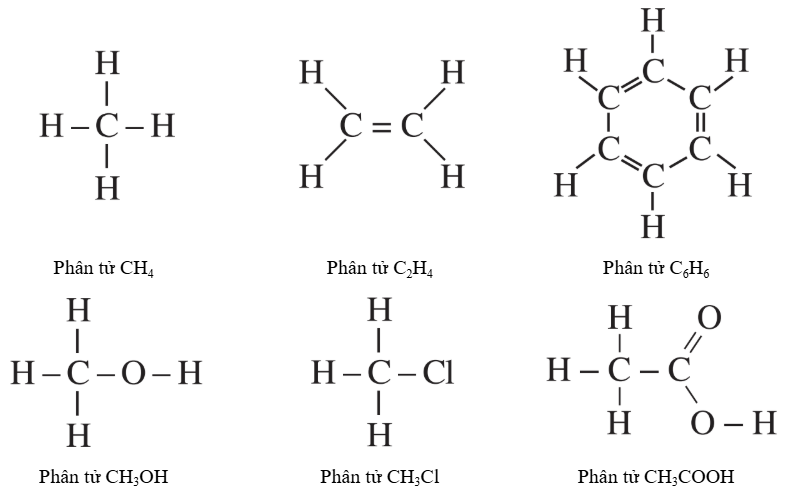
- Hydrocarbon:
+ Phân tử chỉ gồm hai nguyên tố là cacbon và hiđro.
+ Ví dụ: CH₄, C₂H₄, C₆H₆,…
- Dẫn xuất của hydrocarbon:
+ Trong phân tử, ngoài nguyên tố cacbon còn có các nguyên tố khác như O, N, Cl,…
+ Thường có nhóm chức đặc trưng.
+ Ví dụ: C₂H₆O, C₂H₅Cl, CH₃COOH, C₂H₅NH₂,…
3. Hóa học hữu cơ
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu về các hợp chất hữu cơ và những chuyển đổi của chúng.
II. ĐẶC ĐIỂM CẤU TẠO PHÂN TỬ HỢP CHẤT HỮU CƠ
1. Hóa trị và liên kết giữa các nguyên tử
- Trong hợp chất hữu cơ, liên kết chủ yếu là liên kết cộng hóa trị.
- Hóa trị của các nguyên tố thường gặp:
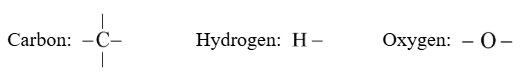
+ Cacbon (C): IV + Hiđro (H): I + Oxi (O): II
- Nguyên tử C có 4 electron lớp ngoài cùng, liên kết với nguyên tử khác bằng cách góp chung electron.
Ví dụ:
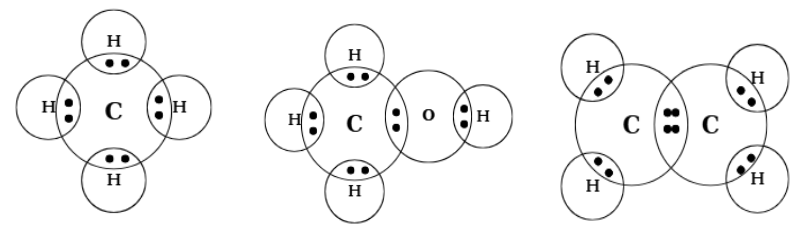
a) CH₄ (methan) b) CH₃OH (metylic ancol) c) C₂H₄ (etilen)
- Liên kết giữa hai nguyên tử bằng 1 cặp electron chung: liên kết đơn.
- Liên kết giữa hai nguyên tử bằng 2 cặp electron chung: liên kết đôi.
- Liên kết đơn: biểu diễn bằng 1 gạch nối (–).
- Liên kết đôi: biểu diễn bằng 2 gạch nối (=).
⇒ Trong hợp chất hữu cơ, cacbon luôn có hóa trị IV.
2. Mạch carbon
- Mạch hở, không phân nhánh:
![]()
- Mạch hở, phân nhánh:
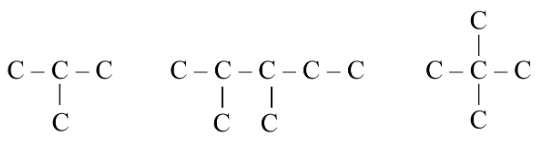
- Mạch vòng:
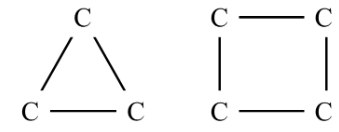
Ví dụ biểu diễn liên kết:
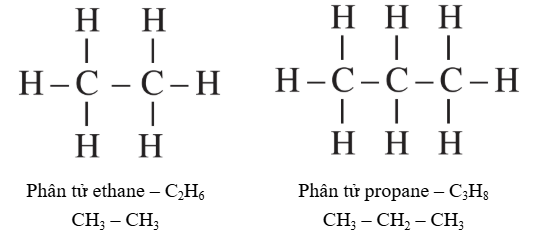
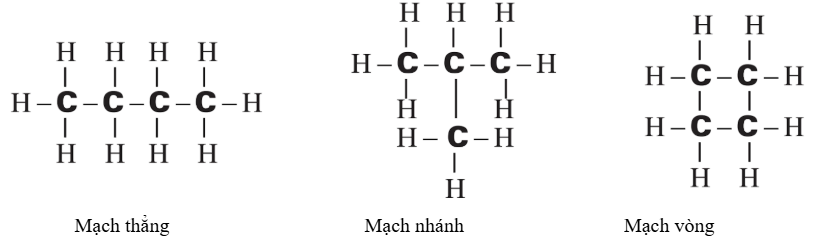
3. Trật tự liên kết giữa các nguyên tử trong phân tử
- Mỗi hợp chất hữu cơ có một trật tự liên kết xác định giữa các nguyên tử trong phân tử.
- Sự thay đổi trật tự liên kết giữa các nguyên tử sẽ làm thay đổi tính chất của hợp chất hữu cơ.
Ví dụ: cùng công thức phân tử C₂H₆O nhưng có hai trật tự liên kết khác nhau:
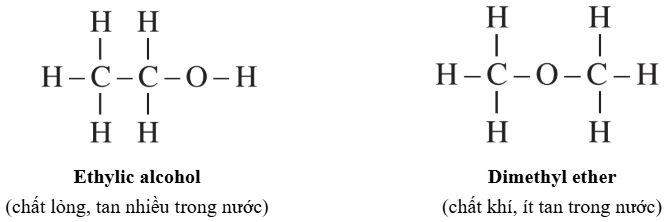
⇒ Cùng công thức phân tử nhưng khác cấu tạo → tính chất vật lý và hóa học khác nhau.
III. CÔNG THỨC PHÂN TỬ VÀ CÔNG THỨC CẤU TẠO
1. Công thức phân tử
- Là công thức cho biết thành phần nguyên tố và số nguyên tử của mỗi nguyên tố trong hợp chất hữu cơ.
- Ví dụ: CH₄, C₂H₆, C₃H₉N, C₂H₆O,…
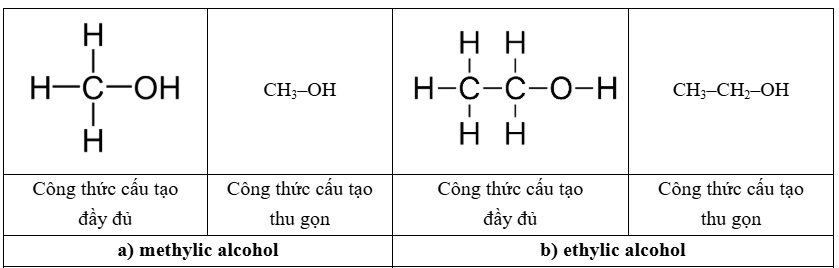
2. Công thức cấu tạo
- Là công thức biểu diễn liên kết giữa các nguyên tử trong phân tử.
- Cho biết trật tự liên kết và cách thức liên kết giữa các nguyên tử.