CẤU TRÚC CỦA CHẤT – SỰ CHUYỂN THỂ
CẤU TRÚC CỦA CHẤT – SỰ CHUYỂN THỂ
Tóm tắt lý thuyết
1. Mô hình động học phân tử về cấu tạo chất
Mô hình động học phân tử về cấu tạo chất bao gồm những nội dung sau:
Các chất được cấu tạo từ các hạt riêng biệt, gọi là phân tử.
Các phân tử luôn chuyển động một cách hỗn độn và không ngừng. Khi nhiệt độ của vật tăng thì tốc độ chuyển động của các phân tử cấu tạo nên vật càng lớn.
Giữa các phân tử tồn tại lực tương tác bao gồm:
Lực hút: chiếm ưu thế khi các phân tử ở xa nhau.
Lực đẩy: chiếm ưu thế khi các phân tử ở gần nhau.
→ Hai lực này được gọi chung là lực liên kết phân tử.
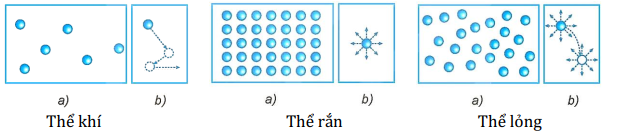
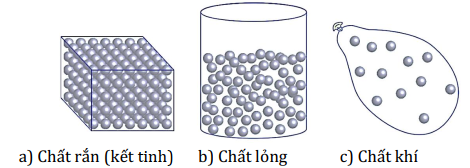
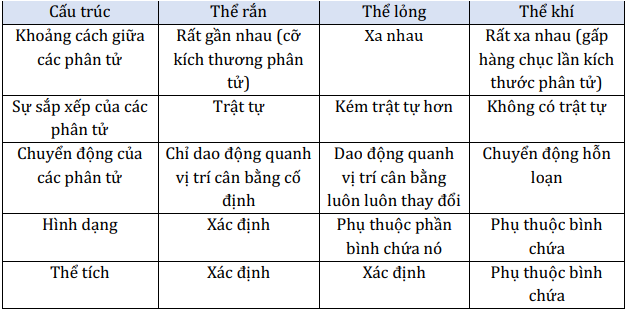
2. Cấu trúc của chất rắn, chất lỏng, chất khí
Dựa vào các đặc điểm sau của phân tử, ta có thể xác định sơ lược cấu trúc của phần lớn các chất rắn, chất lỏng và chất khí:
Khi khoảng cách giữa các phân tử lớn, thì lực liên kết giữa chúng yếu.
Khi các phân tử được sắp xếp có trật tự, thì lực liên kết giữa chúng mạnh.
3. Sự chuyển thể
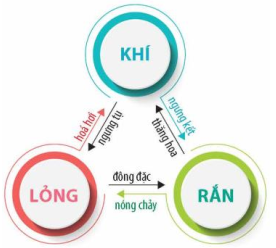
a. Sự chuyển thể
Khi các điều kiện nhiệt độ và áp suất thay đổi, chất có thể chuyển từ thể này sang thể khác.
Các quá trình chuyển thể phổ biến:
Nóng chảy: chuyển từ thể rắn sang thể lỏng.
Đông đặc: chuyển từ thể lỏng sang thể rắn.
Hóa hơi: chuyển từ thể lỏng sang thể khí (hơi).
Ngưng tụ: chuyển từ thể khí (hơi) sang thể lỏng.
Thăng hoa: một số chất rắn như iốt, băng phiến, đá khô (CO₂ ở thể rắn) có thể chuyển trực tiếp sang thể hơi khi nhận nhiệt mà không qua thể lỏng. → Hiện tượng này được gọi là sự thăng hoa. Ngược lại, quá trình từ hơi sang rắn được gọi là ngưng kết.
b. Dùng mô hình động học phân tử giải thích sự chuyển thể
Sự hóa hơi có thể xảy ra dưới hai hình thức: bay hơi và sôi.
Bay hơi là sự hóa hơi xảy ra ở mặt thoáng của chất lỏng. → Ví dụ: Nước trong một cốc không đậy kín sẽ cạn dần.
Cơ chế bay hơi theo mô hình động học phân tử: Do các phân tử chuyển động hỗn loạn và va chạm với nhau, chúng có thể truyền năng lượng cho nhau. Một số phân tử gần mặt thoáng có thể đạt được động năng đủ lớn để thoát khỏi lực hút của các phân tử khác trong chất lỏng. Khi đó, chúng thoát ra khỏi mặt thoáng và trở thành phân tử hơi.
Sự sôi
Khi tiếp tục đun, số phân tử chất lỏng nhận được năng lượng để bứt ra khỏi khối chất lỏng tăng dần, nhiều hơn số phân tử khí (hơi) ngưng tụ.
Khi đó, chất lỏng hóa hơi mạnh mẽ, chuyển dần thành chất khí.
Trong quá trình này, nhiệt độ của chất lỏng tăng dần. Nếu nhận đủ nhiệt lượng, chất lỏng sôi.
Khi sôi, quá trình hóa hơi diễn ra ở cả trong lòng và trên bề mặt chất lỏng.
Sự nóng chảy
Khi nung nóng một vật rắn kết tinh, các phân tử bên trong nhận nhiệt và dao động mạnh hơn, làm khoảng cách giữa các phân tử tăng lên.
Khi nhiệt độ tăng tới một ngưỡng nhất định, một số phân tử thoát khỏi lực liên kết, bắt đầu quá trình nóng chảy.
Trong suốt quá trình này, mặc dù vật rắn tiếp tục nhận nhiệt, nhưng nhiệt độ không thay đổi → vì năng lượng được dùng để phá vỡ liên kết chứ không phải để nâng nhiệt độ.
Khi trật tự của mạng tinh thể bị phá vỡ hoàn toàn, vật chuyển từ trạng thái rắn sang chất lỏng.
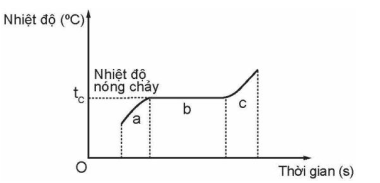
Hình 1.5 – Đồ thị sự thay đổi nhiệt độ của chất rắn khi nung nóng
Giai đoạn a: Chất rắn chưa nóng chảy, nhiệt độ tăng đều.
Giai đoạn b: Chất rắn đang nóng chảy, nhiệt độ không đổi.
Giai đoạn c: Chất rắn đã nóng chảy hoàn toàn, chất lỏng tiếp tục tăng nhiệt độ.
c. Chất rắn kết tinh và chất rắn vô định hình
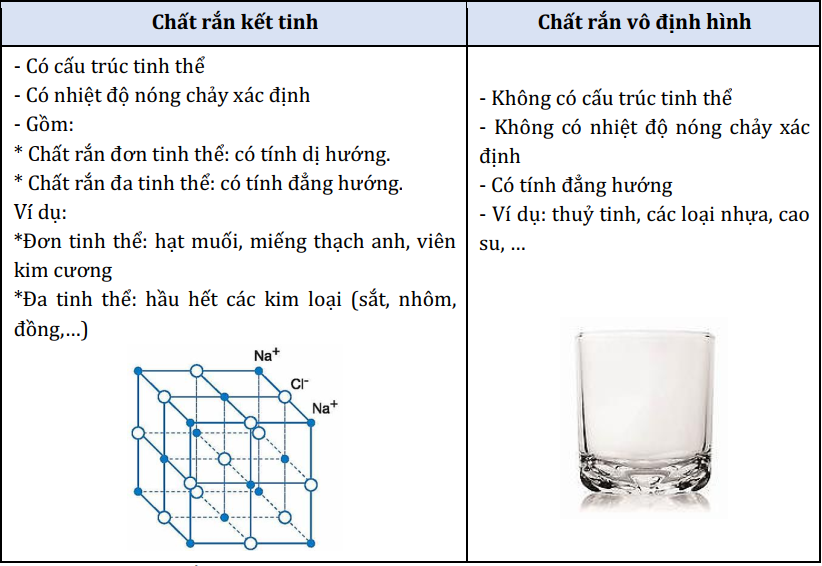
Lưu ý: Một số chất rắn như đường, lưu huỳnh,…có thể tồn tại ở dạng tinh thể hoặc vô định hình.
